f #note
La nature des liasons
Une molecule est une union d’atomes, indentique ou différents, par des liasons chimique. Une liason chimique est causée par l’interaction entre les électrons de valence des atomes en jeu. Les atomes tent d’acquérir la configuration électronique des gax inertes, c’est dire 8 électron de valence . Ont dit donc qu’ils sont régis par la regle de l’octet.
| Famille | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
|---|---|---|---|---|---|---|---|---|
| Nbr d’électron de valence | 1 e- | 2 e- | 3 e- | 4 e- | 5 e- | 6 e- | 7 e- | 8 e- |
| Représenation de lewis |  |  | 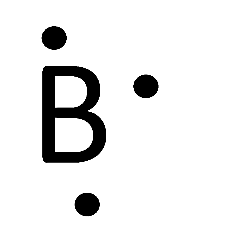 | 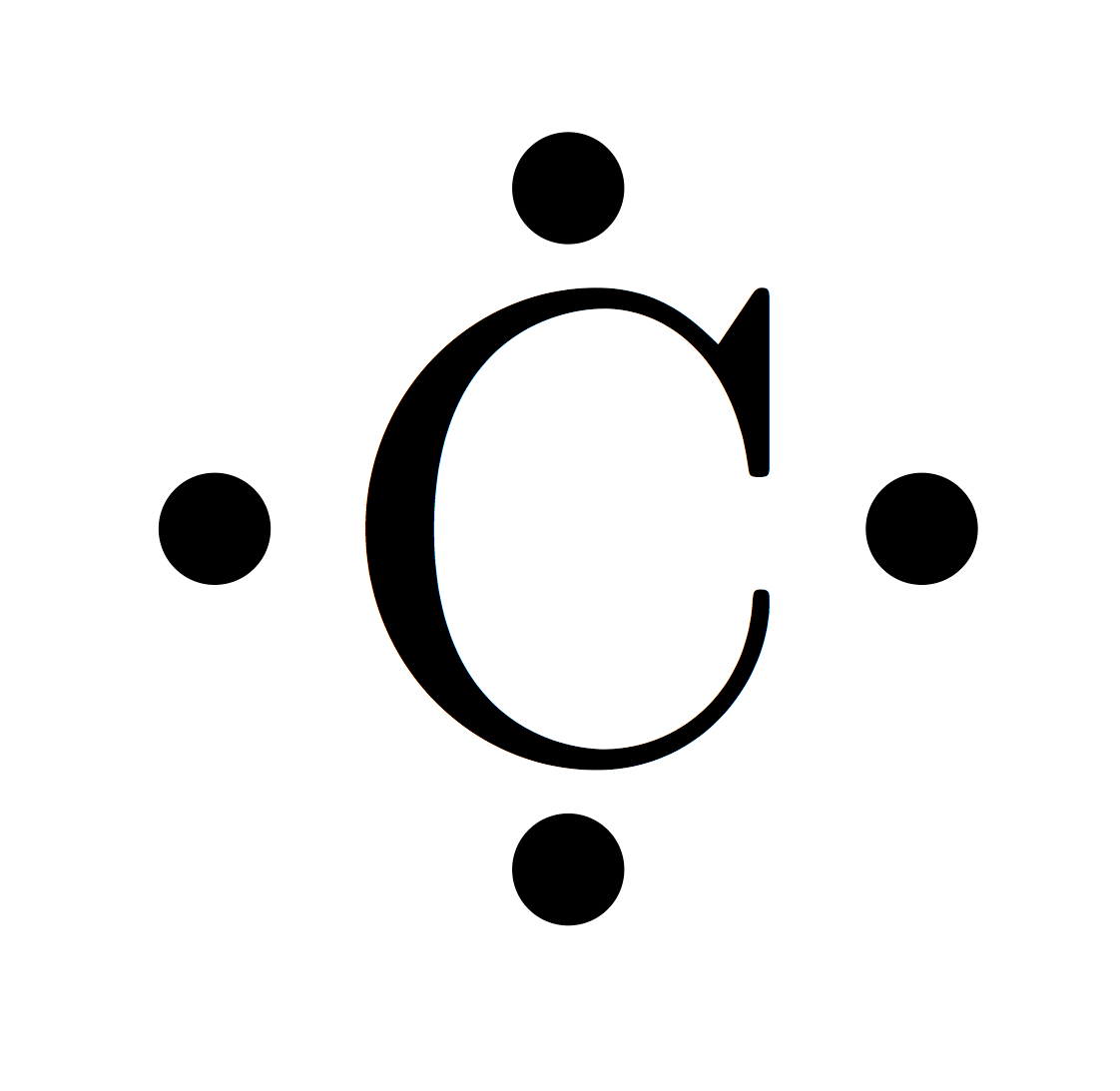 |  |  |  |  |
| Nombre de liason | 1 | 2 | 3 | 4 | 3 | 2 | 1 | 0 |
Les liason chimique sont formet quant un atome “partage” les electrons de valence d’un autre atome. En général, la liason entre deux atomes crée un composeé pls stable que quacun des atomes individuel. Il existe de nombreux types de liason chimique, mais les deux principeaux sont :
Protocole pour déterminer le type de liason :
graph TD 1("Molécule fomrer d'au moins 2 éléments") 2(Élements identique) 3(Élements diferents) 4("Liason covalente") 5("Non métal et non métal") 6("Métal et non métal ") 7("Liason ionique") 1 --> 2 1 --> 3 2 --> 4 3 --> 5 3 --> 6 5 --> 4 6 --> 7
En résumé, les liaisons chimiques sont formées lorsque les atomes partagent des électrons. Il existe deux types principaux de liaisons chimiques : les liaisons covalentes, où les atomes partagent les électrons de manière égale, et les liaisons ioniques, où un métal et un non-métal échangent des électrons. Les liaisons covalentes peuvent être formées entre des atomes du même élément ou des éléments différents. Les liaisons ioniques sont formées entre un métal et un non-métal, ce qui résulte dans la transfert d’électrons et la formation d’ions chargés de signes opposés.